تحديثات الأبحاث 2022-2023
يبقى البحث لتحسين نوعية حياة مجتمعنا بمثابة التزام بالنسبة لنا كمنظمة. نحن نقوم بهذا العمل من خلال صندوق بولين هـ. سيجل Eclipse للأبحاث وبرنامج زمالة جيمس ت. لوبين للأطباء والعلماء.
نحن متحمسون لمشاركة بعض التقدم البحثي معك.
فهم السبب
الوراثة والمؤشرات الحيوية
في عام 2022، حصلت الدكتورة مونيك أندرسون على منحة بحثية لمواصلة البحث مع الدكتور مايكل ليفي الذي يركز على علم الوراثة وتشخيص التهاب النخاع المستعرض. في عمله السابق، اكتشف الدكتور ليفي طفرة (أو تغييرًا) في جين VPS37A لدى ثمانية مرضى مصابين بالتهاب النخاع المستعرض. يصنع VPS37A بروتينًا مهمًا لإعادة تدوير البروتينات وإزالتها من الخلايا. يتم وضع بعض هذه البروتينات في الفضاء خارج الخلايا في أكياس، بعضها يسمى الإكسوسومات. الدكتور ليفي والدكتور أندرسون ليسا متأكدين بعد من كيفية تأثير التغييرات في هذه العملية على التهاب النخاع المستعرض. قد تؤدي التغيرات في هذا الجين إلى إخراج البروتينات خارج الخلية عندما لا يكون من المفترض أن تكون كذلك. قد يتفاعل الجهاز المناعي بعد ذلك مع هذا الخلل بطريقة تسبب التهاب الحبل الشوكي. ومن المثير للاهتمام، أن هذه الطفرة يبدو أنها تزيد من خطر إصابة شخص ما بالتهاب النخاع المستعرض أحادي الطور، مما يعني أن هؤلاء المرضى لديهم نوبة واحدة فقط.
تبحث دراسة الدكتور أندرسون فيما إذا تم العثور على علامات جديدة داخل الإكسوسومات في دم المرضى الذين يعانون من التهاب النخاع المستعرض. من الممكن استخدام هذه العلامات في تشخيص التهاب النخاع المستعرض. ويأمل الباحثون أيضًا في فهم مسارات الإشارات بين الخلايا التي تؤدي إلى استجابة مناعية ضد الحبل الشوكي بشكل أفضل. تشمل الدراسة كلا من المرضى الذين يعانون من التهاب النخاع المستعرض مجهول السبب (بمعنى أنه لم يتم العثور على سبب حتى الآن) والمرضى الذين يعانون من التصلب المتعدد (MS)، ومرض الأجسام المضادة للبروتين السكري قليل التغصن المايلين (MOGAD)، واضطراب طيف التهاب النخاع والعصب البصري (NMOSD). ويأمل الدكتور أندرسون في تحديد ما إذا كانت هناك أي آليات مشتركة بين هذه الأمراض وما إذا كانت هناك بروتينات مماثلة داخل الإكسوسومات يستجيب لها الجهاز المناعي.
في بودكاست "اسأل الخبير". في حلقة SRNA، يوضح الدكتور أندرسون أنه "إذا كانت هناك طفرات مماثلة تحدث في مجموعات مختلفة من المرضى، فقد يعطينا ذلك فكرة عن شيء ما... يحدث في هذه الأمراض المماثلة. لذا، فهو يعطينا فكرة، أولاً، هل هناك اختبارات جينية إضافية ينبغي علينا إجراؤها للمرضى؟ والسؤال الثاني، هل هذا هدف علاجي محتمل لهؤلاء المرضى؟ وتسلط الدكتورة أندرسون الضوء أيضًا على أن مسار الإشارة الذي تتم دراسته ذو صلة بأمراض عصبية أخرى، وأنها تأمل أن توجه الدراسة علاجات التهاب النخاع المستعرض في المستقبل. على حد تعبيرها، "... نفس هذا المسار قد تورط في العديد من الاضطرابات العصبية الأخرى، وخاصة في مجال الإصلاح والتعافي. لذلك، من غير الواضح ما إذا كان هذا هو الحال أيضًا مع التهاب النخاع المستعرض، ولكن هذا شيء نأمل في الإجابة عليه أيضًا.
في عام 2023، د. حصل أندرسون ومايكل ليفي على جائزة NIH R01 بقيمة 1.25 مليون دولار للتعمق في هذه الطفرة الجينية وربما تحديد أهداف جديدة للعلاج. إن الفهم الأفضل لكيفية حدوث أمراض مثل التهاب النخاع المستعرض سيحسن قدرتنا على تشخيصها وعلاجها وربما الوقاية منها.
*مقتطف من مدونة كتبتها هانا كيلي، المتطوعة في جمعية Siegel Rare Neuroimmune Association.
أسباب الاعتلال النقوي
في عام 2022، نشرت زميلة جيمس تي لوبين السابقة في SRNA، الدكتورة أولوين مورفي، مقالًا في مجلة العلوم العصبية، "تحديد الأسباب المحددة للاعتلال النخاعي في مجموعة كبيرة من المرضى الذين تم تشخيص إصابتهم في البداية بالتهاب النخاع المستعرض" مع معلمها الدكتور كارلوس باردو. . يحدد هذا البحث التشخيص المسبب للمرض لدى الأفراد الذين يقدمون اعتلال النخاع إلى مركز جونز هوبكنز لالتهاب النخاع والاعتلال النخاعي بين عامي 2006 و2021 لتقييم "التهاب النخاع المستعرض". تم تحديد التشخيص النهائي بعد إجراء تقييم شامل لكل مريض وتمت مراجعته والتحقق من صحته. من بين 1193 مريضًا، تم تحديد 772 (65٪) لديهم اعتلال نخاعي التهابي، و421 (35٪) لديهم اعتلال نخاعي غير التهابي. كان التصلب المتعدد / المتلازمة المعزولة سريريًا (ن = 221، 29٪) والتهاب النخاع مجهول السبب (ن = 149، 19٪) من أكثر التشخيصات الالتهابية شيوعًا. كان احتشاء الحبل الشوكي (ن = 197، 47٪) والأسباب الهيكلية للاعتلال النخاعي (ن = 108، 26٪) من أكثر التشخيصات غير الالتهابية شيوعًا. بالمقارنة مع الأفراد الذين يعانون من اعتلال النخاع الالتهابي، فإن أولئك الذين يعانون من اعتلال النخاع غير الالتهابي كانوا أكثر عرضة لأن يكونوا أكبر سنا وذكورا ويعانون من تطور الأعراض المزمنة. كانت البداية المفرطة الحدة (أقل من ست ساعات من ظهور الأعراض إلى أسوأ الأعراض العصبية) أكثر شيوعًا لدى المصابين باحتشاء النخاع الشوكي (74٪). في المقابل، كان تطور الأعراض المزمنة أكثر شيوعًا لدى الأفراد الذين يعانون من أسباب هيكلية مثل اعتلال النخاع (81%)، والناسور الشرياني الوريدي أو التشوه الشرياني الوريدي (81%)، والاعتلال النخاعي المرتبط بالاضطرابات الروماتيزمية (71%)، والاعتلال النخاعي المرتبط بالساركويد (61%). . ووجدوا أن معظم الذين تم تشخيص إصابتهم في البداية بـ "التهاب النخاع المستعرض" وجدوا في النهاية أن لديهم سببًا التهابيًا أكثر تحديدًا أو حتى غير التهابي. وهذا يمكن أن يؤدي إلى علاج غير مناسب.
تحسين التشخيص
تقييم المعرفة الخاصة بالحالة لدى المرضى الذين يعانون من اضطرابات المناعة العصبية النادرة
في عام 2022، منحت SRNA منحة بحثية لصندوق Eclipse Fund لزميل SRNA السابق جيمس تي لوبين، الدكتور كايل بلاكبيرن، الأستاذ المساعد في قسم طب الأعصاب في مركز UT Southwestern الطبي من أجل "تقييم المعرفة الخاصة بالحالة لدى المرضى الذين يعانون من اضطرابات المناعة العصبية النادرة (RNDs) )." تتضمن هذه الدراسة مرحلتين. في المرحلة الأولى، تم تطوير مقياس المعرفة الخاصة بحالة RND (مع أسئلة حول RNDs على نطاق واسع بالإضافة إلى مجموعة فرعية من الأسئلة لكل اضطراب) من قبل أطباء متعددي التخصصات وأعضاء فريق جمعية Siegel Rare Neuroimmune Association (SRNA) ). يحتوي هذا الإجراء على أسئلة لتقييم معرفة المشاركين بتشخيص أعراض RND والتشخيص. تم اختبار هذا الإجراء ميدانيًا على عينة صغيرة من المرضى في مركز UT الجنوبي الغربي الطبي. وبناء على ردود الفعل، تم تنقيح الأداة.
خلال المرحلة الثانية القادمة، سيتم تقييم الأداة الجديدة لدى المرضى الذين يعانون من RND (يقدر العدد = 100). نقطة النهاية الأولية للدراسة هي تحديد المعرفة الخاصة بالحالة لدى المصابين بـ RND. سيتم استخدام البيانات التي تم جمعها في هذه الدراسة لتحديد الفجوات المعرفية في هذه الفئة من السكان، والتي ستستفيد منها الجهود التعليمية المستقبلية.
نقص المناعة المتغير المشترك ومتلازمة سجوجرن
نشر زميل جيمس تي لوبين السابق والأستاذ المساعد في علم الأعصاب بجامعة يوتا، الدكتور جوناثان جالي، مقالتين في مجلات علم الأعصاب في عام 2023 مع معلمه الدكتور ستايسي كلاردي. باستطاعتك العثور "المظاهر العصبية لنقص المناعة المتغير الشائع: التأثير على نوعية الحياة" في علم الأعصاب: علم المناعة العصبية والالتهاب العصبي، و "التورط العصبي في متلازمة سجوجرن الأولية المصلية مع خزعة الغدة اللعابية البسيطة الإيجابية: تجربة مركز واحد" في الحدود في علم الأعصاب.
مراجعة السجلات السريرية NMOSD
في عام 2023، شارك مدير الأبحاث والبرامج في SRNA، جي جي ديفيبر، في تأليف ورقتين بحثيتين منشورتين في مجلة علم الأعصاب والعلاج.
الورقة الأولى ، "فهم قرارات العلاج في اضطراب طيف التهاب النخاع والعصب البصري: مراجعة السجلات السريرية العالمية مع مقابلات مع المرضى،" سعى إلى إلقاء نظرة ثاقبة على ممارسات علاج اضطراب طيف التهاب النخاع والعصب البصري (NMOSD) في جميع أنحاء العالم. أكمل أطباء الأعصاب من الولايات المتحدة الأمريكية وألمانيا وإيطاليا والبرازيل وكوريا الجنوبية والصين دراسة استقصائية عبر الإنترنت وقدموا سجلات سريرية للأكوابورين -4 (AQP4) الغلوبولين المناعي G (IgG) - البالغين المصابين بـ NMOSD، والتي تضمنت التركيبة السكانية للمريض والتشخيص والصيانة. تاريخ العلاج، حدوث الانتكاس، وشدته. وأجريت مقابلات مع المرضى الذين يتلقون العلاج الصيانة NMOSD حول التشخيص والعلاج والتصورات حول شدة الانتكاس أو استقرار المرض، ومفاتيح العلاج. قدم ما مجموعه 389 من أطباء الأعصاب سجلات سريرية لـ 1185 مريضًا يعانون من NMOSD إيجابي المصل AQP4-IgG وتمت مقابلة 33 مريضًا يعانون من NMOSD. ما يقرب من 25٪ (228/910) من المرضى من مراجعة السجلات السريرية (CRR) تم تشخيصهم بشكل خاطئ في البداية و 24٪ (8/33) من المرضى الذين تمت مقابلتهم أبلغوا عن تشخيص خاطئ. وارتبط التشخيص الخاطئ بتأخير العلاج وزيادة الانتكاسات مقارنة بمن يتلقون التشخيص الأولي الصحيح (يعني 3.3 مقابل 2.8). لم يبدأ العلاج الصيانة خلال شهرين لـ 2٪ (47/221) من المرضى من CRR و 472٪ (24/8) من المرضى الذين تمت مقابلتهم. كانت الكورتيكوستيرويدات الفموية/العلاجات المثبطة للمناعة عادةً أول علاج صيانة يتم البدء فيه، باستثناء الولايات المتحدة الأمريكية، حيث كان من المرجح أيضًا وصف الأجسام المضادة وحيدة النسيلة. أثرت شدة الانتكاس على قرار بدء/تغيير العلاج واستخدام الأجسام المضادة وحيدة النسيلة. من بين المرضى الذين تمت مقابلتهم، 33% (76/25) لم يتذكروا أنه كان لديهم خيار العلاج ولم يعرف الكثير منهم الأساس المنطقي لاختيار العلاج.
الورقة الثانية "توصيف شدة المرض واستقراره في NMOSD: مراجعة السجلات السريرية العالمية مع مقابلات مع المرضى،" سعى للحصول على نظرة ثاقبة لتصنيف والعوامل المرتبطة بشدة الانتكاس واستقرار المرض في الممارسة السريرية NMOSD في جميع أنحاء العالم. وأظهرت نفس البيانات كما في الدراسة السابقة أنه لا يوجد إجماع واضح على كيفية تعريف شدة الانتكاس في الممارسة السريرية، مع وجود اختلافات جغرافية في تصنيف الانتكاس. يميل أطباء الأعصاب إلى الاعتماد على التقييمات السريرية عند تحديد مدى خطورة المرض، وينظرون إلى كل انتكاسة على حدة. في المقابل، كان للمرضى وجهة نظر أكثر ذاتية بناءً على التغيرات في حياتهم اليومية ومقارناتها مع الانتكاسات السابقة. وبالمثل، كان هناك انفصال في تعريف استقرار المرض حيث أن الغياب التام للانتكاسات كان أكثر أهمية بالنسبة للمرضى منه بالنسبة لأطباء الأعصاب.
تمت رعاية هذه الدراسات بواسطة F. هوفمان-لاروش.
استعادة الوظيفة
تعد دراسة التحقق من سلامة زرع الخلايا السلفية الدبقية البشرية المقيدة في الأشخاص المصابين بالتهاب النخاع المستعرض في مركز UTSW الطبي في دالاس هي أول دراسة تستكشف استخدام الخلايا الجذعية لإصلاح تلف الحبل الشوكي في التهاب النخاع المستعرض. هذه الخلايا الجذعية قادرة على التطور إلى خلايا تنتج المايلين عند وضعها في الأنسجة البشرية. في الدراسات البحثية، تبين أنه بعد زرعها في النخاع الشوكي للأفراد المصابين بالتهاب النخاع المستعرض، ستنتج هذه الخلايا المايلين. أثبتت الدراسات ما قبل السريرية على الحيوانات سلامة وفعالية الخلايا الجذعية. وافقت إدارة الغذاء والدواء الأمريكية (FDA) على الجهاز الجراحي المستخدم لزرع هذه الخلايا الجذعية في الحبل الشوكي. وبعد التأخير الناجم عن جائحة كوفيد-19، تم تسجيل الفرد الأول في ديسمبر 2022 والثاني في سبتمبر 2023.
"لقد استغرق ما نحن فيه اليوم 20 عامًا حرفيًا. ولذلك، فإن خطوات الوصول إلى تجربة سريرية يمكن أن تكون معقدة، وبالنسبة للعلاجات القائمة على الخلايا، فهي معقدة بشكل خاص. – د. بنجامين جرينبيرج، نائب رئيس الأبحاث السريرية والانتقالية، قسم طب الأعصاب، جامعة تكساس ساوث وسترن.
إذا أظهرت التجربة أن الإجراء آمن وفعال، فسوف يسعى المحققون إلى الحصول على الموافقة لتسجيل المزيد من الأشخاص الذين يعانون من TM. وتتمثل الخطة في تسجيل ما يصل إلى تسعة مرضى في هذه الدراسة. يخضع المرشحون للتجربة لمراجعة شاملة لسجلاتهم الطبية وصورهم قبل زيارة UT Southwestern لفحص المواعيد، والتأكد من استيفائهم لمعايير الاشتمال.
تتضمن الجراحة زرع الخلايا الجذعية في الحبل الشوكي، تليها إقامة قصيرة في المستشفى. بعد ذلك، تتم مراقبة المرضى في العيادات الخارجية على مدى عدة أشهر للتأكد من عدم حدوث سمية من الخلايا الجذعية أو من العلاجات المثبطة للمناعة المطلوبة لمنع رد الفعل المناعي السلبي على الخلايا الجذعية.
حاليًا، الهدف الأساسي من دراسة المرحلة 1/2أ هو تقييم سلامة الإجراء وتحديد الجرعة المناسبة. ستشمل المرحلة التالية، المرحلة 2 ب، عددًا أكبر من الأفراد لإجراء مزيد من التقييم لسلامة الإجراء وفعاليته. نظرًا لأن التهاب النخاع المستعرض هو حالة نادرة وخطيرة، فمن المأمول أن تمنح إدارة الغذاء والدواء الأمريكية الموافقة على العلاج قبل إجراء تجارب لاحقة. للحصول على رؤى إضافية، استكشف هذا فيديو 2023 RNDS يوضح تفاصيل الدراسة.
*مقتطف من مدونة كتبتها هانا كيلي، المتطوعة في جمعية Siegel Rare Neuroimmune Association.
منحة التقدم لـ NMOSD
واصلت الدكتورة ساميتا ساتيانارايان العمل على التمويل البحثي الذي تلقته كجزء من منحة التقدم لـ NMOSD. تمول منحة التقدم الأبحاث التي تهدف إلى تحسين فهم اضطراب طيف التهاب النخاع والعصب البصري (NMOSD)، والتي تركز بشكل خاص على السكان الأمريكيين الآسيويين والأفارقة.
تجري الدكتورة ساميتا ساتيانارايان بحثًا حول "تقييم تأثير الفوارق الاجتماعية الصحية على الإعاقة والحصول على الرعاية لدى مرضى NMOSD." وهي زميلة في علم المناعة العصبية في مستشفى جبل سيناء في مدينة نيويورك، نيويورك. تركز دراستها على تقييم كيفية تأثير عوامل حياة الناس، والتي تسمى المحددات الاجتماعية للصحة، على حصولهم على الرعاية والإعاقة وعملية المرض لدى الأشخاص الذين يعانون من NMOSD.
بعض المحددات الاجتماعية للصحة التي يدرسها الدكتور ساتيانارايان تشمل الوصول إلى التعليم وجودته، والحصول على الرعاية الصحية وجودتها، والأحياء والبيئة المبنية، والسياق الاجتماعي والمجتمعي، والاستقرار الاقتصادي. يمكن أن تؤدي الاختلافات في هذه العوامل إلى اختلافات في عملية المرض، وهو ما يسمى بالتفاوتات. إن الفهم الأفضل لهذه العوامل يمكن أن يساعد المهنيين الطبيين على معالجة الفوارق مع توفير الرعاية للأفراد الذين تم تشخيص إصابتهم بـ NMOSD.
يمكن قياس إمكانية الحصول على الرعاية من خلال الوقت المنقضي بين ظهور الأعراض وحتى التشخيص، والوقت الذي يستغرقه تلقي أول علاج معدّل للمرض، ونوع العلاج المعدل للمرض الذي يتم تلقيه. ومن ناحية أخرى، يتم قياس الإعاقة من خلال النتائج التي أبلغ عنها المريض، مثل حالة التنقل وأنشطة الحياة اليومية؛ الحالة التي أبلغ عنها الطبيب، مثل حالة التمشي؛ درجات الإعاقة الموحدة والمصدق عليها، مثل مقياس حالة الإعاقة الموسع (EDSS) والمشي المحدد بمدة 25 قدمًا؛ وفحص الرؤية وحدة البصر. ستشمل دراسة الدكتور ساتيانارايان كلا من البيانات المستقبلية (البيانات التي تركز على الحاضر والمستقبل) والبيانات الاسترجاعية (البيانات التي تركز على الماضي) وستتضمن بيانات من ثلاثة مراكز طبية أكاديمية - مستشفى ماونت سيناي، وجامعة جنوب كاليفورنيا، وماساتشوستس مستشفى عام. يمكنك معرفة المزيد عن الدراسة البحثية من خلال مشاهدة عرض الدكتور ساتيانارايان في ندوة الاضطرابات المناعية العصبية النادرة (RNDS) لعام 2021.
نحن نتطلع إلى معرفة المزيد عن تأثير الفوارق الصحية لدى الأشخاص الذين يعانون من NMOSD من بحث الدكتور ساتيانارايان، ونأمل أن يؤدي ذلك إلى رعاية أفضل لأولئك الموجودين في مجتمع NMOSD.
زمالة SRNA جيمس ت. لوبين
بالإضافة إلى بعض الأبحاث الموضحة أعلاه، فإننا لا نزال ملتزمين بتمويل المنح الدراسية لتدريب الأطباء والعلماء على اضطرابات المناعة العصبية النادرة.
في 2023، الدكتور هايوين تشين بدأت زمالتها في جامعة جونز هوبكنز تحت إشراف الدكتور كارلوس باردو. الدكتورة تشين هي طبيبة أعصاب أطفال وعالمة أعصاب حصلت على شهادتها الطبية من جامعة ميريلاند. ثم أكملت الإقامة في طب الأطفال في مستشفى جونز هوبكنز في بالتيمور، ماريلاند. إنها مهتمة بفهم كيفية تأثير MOGAD على الخلايا العصبية والخلايا الدبقية قليلة التغصن لتسبب خللًا عصبيًا. وللقيام بذلك، تقوم بتطوير نظام نموذجي في المختبر للخلايا العصبية والدبقية لفحص كيفية تعطيلها بواسطة الأجسام المضادة الذاتية لـ MOGAD والاستجابة الالتهابية المرتبطة بها، حيث يتم تنشيط الخلايا البلعمية والخلايا التائية والخلايا البائية والخلايا الدبقية الصغيرة من خلال إطلاق السيتوكينات. وقد تورطوا جميعا.
قد يساعدنا فهم هذه العملية في فهم كيفية تسبب MOGAD في خلل في الدماغ والعمود الفقري. يمكننا بعد ذلك تصميم استراتيجيات أفضل بذكاء لعلاج المرض. على سبيل المثال، فإن فهم أي جزء من الجهاز المناعي قد يكون مفرط النشاط في MOGAD قد يسمح لنا باستهداف وقمع هذا المكون المعين في الجهاز المناعي بشكل انتقائي للتخفيف من المرض. علاوة على ذلك، سيستخدم الفريق التقنيات المناعية والميتاجينومية للبحث عن حالات العدوى المتزامنة لدى المرضى الذين يعانون من مرض MOGAD للتحقق مما إذا كانت العدوى قد تؤدي إلى تفاعلات مناعية تهدف في البداية إلى مكافحة العدوى التي تهاجم أيضًا خلايا الجسم نفسها، مسببة أمراض المناعة الذاتية، مثل MOGAD. ويفترضون أن نوع مسبب المرض إلى جانب خصائص الجسم المضاد الذاتي لدى المرضى الأفراد، مثل مكان ارتباطه ومدى قوة ارتباطه، قد يوفر نظرة ثاقبة للمسار السريري للمرض. وأخيرًا، سيتحقق الفريق من أسباب اختلاف شدة المرض بين المرضى، ومعدلات الانتكاس المختلفة، والاستجابة المختلفة للعلاجات. ويتوقعون أن هذه المظاهر السريرية قد تكون مرتبطة بمدى خلل خلايا الدماغ الناجم عن المرض وكذلك كيفية تحفيز المرض. إن الفهم الأفضل لكيفية ظهور هذه الاختلافات السريرية سيسمح لنا بأن نكون أكثر قدرة على تقديم المشورة للمرضى بشأن التشخيص ومسار المرض. علاوة على ذلك، من المرجح أن تؤثر التنبؤات الخاصة بخطورة المسار السريري على خيارات الإدارة من حيث مدى قوة علاج المرض لتقليل الإعاقة العصبية مع موازنة المخاطر المحتملة لدورات العلاج المختلفة.
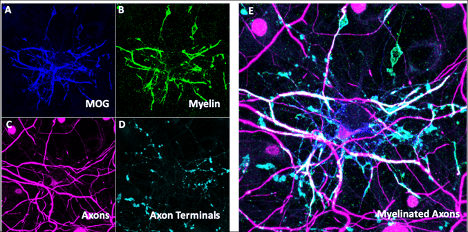
أسطورة الشكل: نموذج في المختبر للخلايا العصبية المايلينية. تُظهر الكيمياء المناعية وجود الخلايا الدبقية قليلة التغصن التي تحمل علامة MOG (A) وMBP (B) والخلايا العصبية التي تحمل علامة NF-H (C) وvGlut1 (D) مع صورة مركبة (E) توضح تداخلها الذي يمثل الأجزاء المايلينية من محاور الخلايا العصبية.
البحوث التي تقودها SRNA
سجل SRNA
الهدف من سجل SRNA والذي بدأ في عام 2016 هو المساعدة في تطوير الأبحاث حول اضطرابات المناعة العصبية النادرة، والتعاون مع باحثين من جميع أنحاء العالم، وتحديد المشاركين في التجارب السريرية.
اعتبارًا من ديسمبر 2023، شارك 711 شخصًا في السجل. لقد أضفنا مؤخرًا أيضًا مكونًا طوليًا إلى السجل والذي سيُطلب من المشاركين ملئه على أساس سنوي. يعد هذا المكون مهمًا لأن تشخيص الأشخاص يتغير أحيانًا، ونريد قياس ما إذا كان هناك أي تغييرات في الأدوية التي يتناولها شخص ما ونوعية حياته.
اعتبارًا من ديسمبر 2023، تم تشخيص إصابة 68% من المشاركين بالتهاب النخاع المستعرض، و10% باضطراب طيف التهاب النخاع والعصب البصري، و4% بالتهاب الدماغ والنخاع الحاد المنتشر، و4% بالتهاب النخاع الرخو الحاد، و9% بمرض الأجسام المضادة MOG، و4% بمرض آخر أو لم يتلقوا بعد التشخيص.
تم تشخيص 35% منهم في أقل من أسبوع واحد من ظهور الأعراض، ولكن بالنسبة لـ 32% من المشاركين، استغرق التشخيص أكثر من ستة أسابيع. تلقى 83% من المشاركين العلاج بعد أول نوبة حادة لهم. ومع ذلك، من بين أولئك الذين تلقوا العلاج الحاد الأول، تلقى 33٪ فقط من المشاركين علاجًا ثانيًا مختلفًا عن الأول. تلقى 76% من المشاركين العلاج التأهيلي.
يعاني 79% من المشاركين حاليًا من الضعف أو الشلل، ويعاني 78% من المشاركين من تنميل أو فقدان الإحساس، ويعاني 62% من المشاركين من التشنج أو التشنجات العضلية غير المنضبطة. يعاني 54% من آلام الرقبة أو الظهر، ويعاني 76% من المشاركين من آلام الأعصاب، ويعاني 69% من المشاركين من أعراض المثانة و/أو الأمعاء.
جودة الحياة (QoL) وإدارة الرعاية المستمرة بين المصابين باضطراب طيف التهاب النخاع والعصب البصري (NMOSD)
الهدف الأساسي لهذه الدراسة هو فهم تجربة وتصورات أولئك الذين يعانون من NMOSD أو شركاء الرعاية الخاصين بهم بشأن نوعية حياتهم فيما يتعلق بإدارتهم المستمرة للرعاية، بما في ذلك الوصول إلى الرعاية الطبية والعلاجات والحواجز المحتملة التي يواجهونها أثناء فترة العلاج. حياتهم فيما يتعلق باضطرابهم.
لقد استكشفنا الأسئلة التالية:
- كيف ينظر الأشخاص الذين لديهم NMOSD أو شركاؤهم في الرعاية إلى جودة الحياة؟
- كيف تبدو رحلة الرعاية المستمرة لأولئك الذين يعانون من NMOSD؟
- كيف يمكننا تصميم برامج وخدمات جديدة تعمل على تحسين جودة الحياة لأولئك الذين يعانون من NMOSD فيما يتعلق بالرعاية المستمرة؟
على حد علمنا، لا توجد دراسات نوعية منشورة تستخدم النتائج التي أبلغ عنها المريض (PROs) من خلال عملية تصميم تتمحور حول الإنسان لتحديد تصورات جودة الحياة لدى الأشخاص الذين يعانون من اضطرابات المناعة العصبية النادرة فيما يتعلق بالرعاية المستمرة. تتضمن المبادئ الأساسية للتصميم الذي يركز على الإنسان الخطوات المتسلسلة التالية: التعاطف مع جميع أصحاب المصلحة؛ عرف المشكلة؛ فكر بطريقة منفتحة. حلول النموذج الأولي؛ والاختبار. يعتمد تطبيقنا للتصميم الذي يتمحور حول الإنسان على إطار نظرية الأساس، حيث يتم تحديد المواضيع خلال سلسلة من المقابلات والأنشطة العملية (على سبيل المثال، دراسة اليوميات)، وجلسة التفكير، وجلسة مراجعة النموذج الأولي. جلسة التفكير هي عملية يتم فيها توليد الأفكار من خلال جلسة جماعية تتضمن أنشطة بصرية مع الآخرين الذين تم تشخيص إصابتهم بـ NMOSD. يعد فهم محفزات وتصورات جودة الحياة أمرًا مهمًا لعملنا كمنظمة لتلبية احتياجات مجتمع المرضى لدينا على أفضل وجه والمشاركة في تطوير الحلول لتحسين إدارة الرعاية المستمرة.
كان لدينا ما مجموعه 58 شخصًا يملأون أداة الفرز، وتم إجراء مقابلات مع 12 شخصًا من قبل طاقم الدراسة. ثم عقدنا ما مجموعه 4 جلسات للتفكير، ثلاث منها مع أفراد يعانون من NMOSD (العدد = 11) وواحدة مع المتخصصين الطبيين الذين يرون المرضى الذين يعانون من NMOSD (العدد = 3). بناءً على المناقشات التي دارت في جلسة التفكير، أنشأ فريق الدراسة "رحلة مريض". لقد شاركنا رحلة المريض هذه في جلسات النماذج الأولية مع 11 فردًا باستخدام NMOSD وسنقوم بنشر النتائج