Onderzoeksupdates 2022-2023
Onderzoek om de levenskwaliteit van onze gemeenschap te verbeteren blijft een verplichting voor ons als organisatie. Wij doen dit werk door Het Pauline H. Siegel Eclipse Fonds voor Onderzoek en het James T. Lubin Clinician-Scientist Fellowship-programma.
We zijn verheugd om enkele onderzoeksvooruitgangen met u te delen.
Oorzakelijk verband begrijpen
Genetica en biomarkers
In 2022 ontving Dr. Monique Anderson een onderzoekssubsidie om samen met Dr. Michael Levy het onderzoek voort te zetten, gericht op genetica en diagnose van transversale myelitis. In zijn eerdere werk ontdekte Dr. Levy een mutatie (of verandering) in het VPS37A-gen bij acht patiënten met transversale myelitis. VPS37A maakt een eiwit dat belangrijk is voor het recyclen en verwijderen van eiwitten uit cellen. Sommige van deze eiwitten worden in de ruimte buiten de cellen in zakjes geplaatst, waarvan sommige exosomen worden genoemd. Dr. Levy en Dr. Anderson weten nog niet zeker hoe veranderingen in dit proces betrokken zijn bij transversale myelitis. Veranderingen in dit gen kunnen ervoor zorgen dat eiwitten buiten de cel worden gebracht terwijl dat niet de bedoeling is. Het immuunsysteem kan dan op deze verstoring reageren op een manier die een ontsteking van het ruggenmerg veroorzaakt. Interessant genoeg lijkt deze mutatie iemands risico op monofasische transversale myelitis alleen maar te vergroten, wat betekent dat deze patiënten slechts één aanval krijgen.
De studie van Dr. Anderson onderzoekt of er nieuwe markers in exosomen worden gevonden in het bloed van patiënten met transversale myelitis. Deze markers kunnen mogelijk worden gebruikt bij de diagnose van transversale myelitis. De onderzoekers hopen ook de signaalroutes tussen cellen die een immuunrespons tegen het ruggenmerg veroorzaken beter te begrijpen. De studie omvat zowel patiënten met idiopathische transversale myelitis (wat betekent dat er nog geen oorzaak is gevonden) als patiënten met multiple sclerose (MS), myeline-oligendrocytglycoproteïne-antilichaamziekte (MOGAD) en neuromyelitis optica spectrumstoornis (NMOSD). Dr. Anderson hoopt te bepalen of er gemeenschappelijke mechanismen zijn tussen deze ziekten en of er vergelijkbare eiwitten in exosomen zitten waarop het immuunsysteem reageert.
In een Podcast ‘Vraag het aan de expert’ aflevering met SRNA legt Dr. Anderson uit dat “als er vergelijkbare mutaties voorkomen in de verschillende patiëntenpopulaties, dat ons een aanwijzing zou kunnen geven over iets dat…voorkomt bij deze vergelijkbare ziekten. Het geeft ons dus een idee van: zijn er aanvullende genetische tests die we voor patiënten zouden moeten doen? En ten tweede: is dit een potentieel therapeutisch doelwit voor deze patiënten?” Dr. Anderson benadrukt ook dat de signaalroute die wordt bestudeerd relevant is voor andere neurologische ziekten en dat ze hoopt dat de studie toekomstige therapieën voor transversale myelitis zal begeleiden. In haar woorden: “…datzelfde… pad is betrokken bij verschillende andere neurologische aandoeningen, vooral op het gebied van herstel en herstel. Het is dus onduidelijk of dit ook het geval zal zijn bij myelitis transversa, maar dit is iets dat we ook hopen te beantwoorden.”
In 2023 heeft drs. Anderson en Michael Levy ontvingen een NIH R01-prijs van $ 1.25 miljoen om dieper in deze genetische mutatie te graven en mogelijk nieuwe doelwitten voor therapie te identificeren. Een beter begrip van hoe ziekten zoals myelitis transversa ontstaan, zal ons vermogen verbeteren om ze te diagnosticeren, behandelen en misschien te voorkomen.
*Overgenomen uit een blog geschreven door Hannah Kelly, een vrijwilliger voor de Siegel Rare Neuroimmune Association.
Oorzaken van myelopathie
In 2022 publiceerde voormalig SRNA James T. Lubin Fellow Dr. Olwen Murphy een artikel in de Journal of Neurological Sciences, “Identificatie van specifieke oorzaken van myelopathie in een groot cohort van patiënten die aanvankelijk werden gediagnosticeerd met transversale myelitis” met haar mentor Dr. Carlos Pardo . Dit onderzoek identificeert de etiologische diagnose bij personen die zich tussen 2006 en 2021 met myelopathie presenteren aan het Johns Hopkins Myelitis and Myelopathy Center voor evaluatie van ‘transverse myelitis’. De definitieve diagnose werd vastgesteld na een uitgebreide evaluatie van elke patiënt en werd beoordeeld en gevalideerd. Van de 1193 geïncludeerde patiënten werd bij 772 (65%) vastgesteld dat ze een inflammatoire myelopathie hadden, en bij 421 (35%) werd vastgesteld dat ze een niet-inflammatoire myelopathie hadden. Multiple sclerose/klinisch geïsoleerd syndroom (n = 221, 29%) en idiopathische myelitis (n = 149, 19%) waren de meest voorkomende inflammatoire diagnoses. Ruggenmerginfarct (n = 197, 47%) en structurele oorzaken van myelopathie (n = 108, 26%) waren de meest voorkomende niet-inflammatoire diagnoses. Vergeleken met individuen met inflammatoire myelopathieën, was de kans groter dat degenen met niet-inflammatoire myelopathieën ouder en mannelijk waren en chronische symptoomevolutie vertoonden. Hyperacuut begin (minder dan zes uur vanaf het begin van de symptomen tot de ergste neurologische symptomen) kwam het vaakst voor bij mensen met een ruggenmerginfarct (74%). Daarentegen kwam de evolutie van chronische symptomen het meest voor bij personen met structurele oorzaken van myelopathie (81%), arterioveneuze fistel of arterioveneuze malformatie (81%), myelopathie geassocieerd met reumatologische aandoeningen (71%) en sarcoïdose-geassocieerde myelopathie (61%). . Ze ontdekten dat de meeste mensen bij wie aanvankelijk de diagnose ‘transversale myelitis’ werd gesteld, uiteindelijk een meer specifieke inflammatoire of zelfs niet-inflammatoire oorzaak bleken te hebben. Dit kan mogelijk leiden tot een ongepaste behandeling.
Verbetering van de diagnose
Conditiespecifieke kennis beoordelen bij patiënten met zeldzame neuro-immuunziekten
In 2022 kende SRNA een Eclipse Fund Research Grant toe aan voormalig SRNA James T. Lubin Fellow Dr. Kyle Blackburn, assistent-professor bij de afdeling Neurologie van het UT Southwestern Medical Center voor “Het beoordelen van conditiespecifieke kennis bij patiënten met zeldzame neuro-immuunziekten (RND’s). ).” Dit onderzoek omvat twee fasen. In de eerste fase werd een maatstaf voor de aandoeningspecifieke kennis van RND (met vragen over RND's in grote lijnen en een subset van vragen voor elke aandoening) ontwikkeld door multidisciplinaire artsen en teamleden van de Siegel Rare Neuroimmune Association (SRNA). ). Deze maatstaf bevat vragen om de kennis van de deelnemers over de diagnose van RND-symptomen en de prognose te beoordelen. De maatregel werd in de praktijk getest bij een kleine steekproef van patiënten in het UT Southwestern Medical Center. Op basis van de feedback is het instrument herzien.
Tijdens een komende tweede fase zal het nieuwe instrument worden beoordeeld bij patiënten met RND (geschatte n=100). Het primaire eindpunt van het onderzoek is het bepalen van de aandoeningspecifieke kennis bij mensen met RND. De in dit onderzoek verzamelde gegevens zullen worden gebruikt om kennishiaten in deze populatie te identificeren, wat toekomstige onderwijsinspanningen zal informeren.
Gemeenschappelijke variabele immunodeficiëntie en het syndroom van Sjögren
Voormalig James T Lubin Fellow en assistent-professor neurologie aan de Universiteit van Utah, Dr. Jonathan Galli, publiceerde in 2023 twee artikelen in neurologische tijdschriften met zijn mentor Dr. Stacey Clardy. Je kunt vinden “Neurologische manifestaties van gemeenschappelijke variabele immuundeficiëntie: impact op de kwaliteit van leven” in Neurologie: Neuroimmunologie en Neuro-inflammatie, en “Neurologische betrokkenheid bij het seronegatieve primaire syndroom van Sjögren met positieve kleine speekselklierbiopsie: een ervaring in één centrum” in Frontiers in Neurology.”
NMOSD klinische dossierbeoordeling
In 2023 was SRNA's directeur onderzoek en programma's, GG deFiebre, co-auteur van twee artikelen gepubliceerd in het Journal Neurology and Therapy.
Het eerste papier, “Behandelingsbeslissingen begrijpen bij neuromyelitis optica-spectrumstoornis: een mondiaal klinisch overzicht met interviews met patiënten,” zocht naar inzichten in de behandelpraktijken voor neuromyelitis optica spectrum stoornis (NMOSD) wereldwijd. Neurologen uit de VS, Duitsland, Italië, Brazilië, Zuid-Korea en China voltooiden een online enquête en dienden klinische dossiers in voor aquaporine-4 (AQP4) immunoglobuline G (IgG)-seropositieve volwassenen met NMOSD, waaronder demografische gegevens van de patiënt, diagnose en onderhoud behandelgeschiedenis, het optreden van terugval en de ernst ervan. Patiënten die NMOSD-onderhoudstherapie kregen, werden geïnterviewd over hun diagnose, behandeling, percepties over de ernst van de terugval of de stabiliteit van de ziekte, en overschakelingen op de behandeling. In totaal dienden 389 neurologen klinische dossiers in van 1185 patiënten met AQP4-IgG-seropositieve NMOSD en werden 33 patiënten met NMOSD geïnterviewd. Ongeveer 25% (228/910) van de patiënten uit de klinische dossierbeoordeling (CRR) kreeg aanvankelijk een verkeerde diagnose en 24% (8/33) van de geïnterviewde patiënten rapporteerde een verkeerde diagnose. Een verkeerde diagnose ging gepaard met vertraging van de behandeling en meer recidieven vergeleken met degenen die de juiste initiële diagnose kregen (gemiddeld 3.3 versus 2.8). Onderhoudstherapie werd niet binnen 2 maanden gestart voor 47% (221/472) van de patiënten uit de CRR en 24% (8/33) van de geïnterviewde patiënten. Orale corticosteroïden/immunosuppressieve therapieën waren doorgaans de eerste onderhoudsbehandeling die werd gestart, behalve in de VS, waar de kans even groot was dat monoklonale antilichamen werden voorgeschreven. De ernst van de terugval beïnvloedde de beslissing om de therapie te starten/wijzigen en monoklonale antilichamen te gebruiken. Van de geïnterviewde patiënten kon 76% (25/33) zich niet herinneren dat zij een behandelingskeuze hadden en velen kenden de redenen voor de behandelingskeuze niet.
Het tweede papier, “Karakterisering van de ernst en stabiliteit van ziekten bij NMOSD: een mondiaal overzicht van klinische dossiers met interviews met patiënten,” zocht naar inzichten in de classificatie van en factoren die verband houden met de ernst van de terugval en de ziektestabiliteit in de klinische praktijk van NMOSD wereldwijd. Uit dezelfde gegevens als uit het eerdere onderzoek bleek dat er geen duidelijke consensus bestond over de manier waarop de ernst van de terugval in de klinische praktijk werd gedefinieerd, met geografische verschillen in de classificatie van terugval. Neurologen waren bij het bepalen van de ernst vaak afhankelijk van klinische beoordelingen en bekeken elke terugval afzonderlijk. Patiënten hadden daarentegen een meer subjectief beeld, gebaseerd op de veranderingen in hun dagelijks leven en vergelijkingen met eerdere recidieven. Op dezelfde manier was er sprake van een discrepantie in de definitie van ziektestabiliteit, in die zin dat de volledige afwezigheid van recidieven belangrijker was voor patiënten dan voor neurologen.
Deze onderzoeken werden gesponsord door F. Hoffmann-La Roche.
Functie herstellen
Het onderzoek naar de veiligheid van de transplantatie van menselijke gliale beperkte voorlopercellen naar proefpersonen met transversale myelitis in het UTSW Medical Center in Dallas is het eerste onderzoek naar het gebruik van stamcellen voor het herstellen van schade aan het ruggenmerg bij transversale myelitis. Deze stamcellen kunnen zich ontwikkelen tot cellen die myeline produceren wanneer ze in menselijk weefsel worden geplaatst. In onderzoeken is aangetoond dat deze cellen, nadat ze zijn getransplanteerd in het ruggenmerg van personen met transversale myelitis, myeline zullen produceren. Preklinische onderzoeken bij dieren hebben de veiligheid en werkzaamheid van de stamcellen aangetoond. De FDA heeft het chirurgische apparaat goedgekeurd dat wordt gebruikt om deze stamcellen in het ruggenmerg te implanteren. Na een vertraging als gevolg van de COVID-19-pandemie werd de eerste persoon in december 2022 en de tweede in september 2023 ingeschreven.
“Waar we nu staan, is letterlijk twintig jaar in de maak geweest. En dus kunnen de stappen om tot een klinische proef te komen ingewikkeld zijn, en voor celgebaseerde therapieën zijn ze bijzonder ingewikkeld.” – Dr. Benjamin Greenberg, vicevoorzitter voor klinisch en translationeel onderzoek, afdeling neurologie, Universiteit van Texas Southwestern.
Als uit het onderzoek blijkt dat de procedure veilig en effectief is, zullen de onderzoekers goedkeuring vragen om meer mensen met TM in te schrijven. Het plan is om maximaal negen patiënten in deze studie te betrekken. Kandidaten voor de proef ondergaan een grondige beoordeling van hun medische dossiers en beeldvorming voordat ze UT Southwestern bezoeken voor screeningafspraken, om er zeker van te zijn dat ze aan de inclusiecriteria voldoen.
De operatie omvat het implanteren van stamcellen in het ruggenmerg, gevolgd door een kort verblijf in het ziekenhuis. Daarna worden patiënten gedurende een periode van enkele maanden in poliklinieken gevolgd om er zeker van te zijn dat er geen toxiciteit optreedt door de stamcellen of door de immunosuppressieve therapieën die nodig zijn om een ongunstige immuunreactie op de stamcellen te voorkomen.
Momenteel is het primaire doel van deze fase 1/2a-studie het beoordelen van de veiligheid van de procedure en het vaststellen van de juiste dosering. Bij de volgende fase, fase 2b, zullen een groter aantal personen betrokken zijn om de veiligheid en werkzaamheid van de procedure verder te evalueren. Omdat myelitis transversa een zeldzame en ernstige aandoening is, wordt gehoopt dat de FDA goedkeuring zal verlenen voor de therapie voordat er vervolgstudies worden uitgevoerd. Voor meer inzichten kunt u dit verkennen RNDS-video uit 2023 met details over het onderzoek.
*Overgenomen uit een blog geschreven door Hannah Kelly, een vrijwilliger voor de Siegel Rare Neuroimmune Association.
Voortgangsbeurs voor NMOSD
Dr. Sammita Satyanarayan bleef werken aan de onderzoeksfinanciering die ze ontving als onderdeel van de Progress Grant voor NMOSD. De Progress Grant financiert onderzoek gericht op het verbeteren van het begrip van neuromyelitis optica spectrumstoornis (NMOSD), specifiek gericht op Aziatische en Afro-Amerikaanse populaties.
Dr. Sammita Satyanarayan doet onderzoek naar “Het beoordelen van de impact van sociale verschillen in gezondheid op handicaps en toegang tot zorg bij NMOSD-patiënten.” Ze is neuro-immunologiemedewerker in het Mt. Sinai Hospital in New York City, NY. Haar onderzoek is gericht op het evalueren van de manier waarop de factoren van het leven van mensen, sociale determinanten van gezondheid genoemd, hun toegang tot zorg, handicap en ziekteproces beïnvloeden bij mensen met NMOSD.
Enkele van de sociale determinanten van de gezondheid die Dr. Satyanarayan bestudeert zijn onder meer de toegang tot en de kwaliteit van het onderwijs, de toegang en de kwaliteit van de gezondheidszorg, de buurt en de gebouwde omgeving, de sociale en gemeenschapscontext, en economische stabiliteit. Verschillen in deze factoren kunnen leiden tot verschillen in het ziekteproces, die dispariteiten worden genoemd. Een beter begrip van deze factoren kan medische professionals helpen de verschillen aan te pakken en tegelijkertijd zorg te verlenen aan personen met de diagnose NMOSD.
De toegang tot zorg kan worden gemeten aan de hand van de tijd tussen het begin van de symptomen en de diagnose, de tijd die nodig is om de eerste ziektemodificerende behandeling te krijgen en het type ziektemodificerende therapie dat wordt ontvangen. Handicap daarentegen wordt gemeten aan de hand van door de patiënt gerapporteerde uitkomsten, zoals de ambulante status en de activiteiten van het dagelijks leven; door een arts gerapporteerde status, zoals ambulante status; gestandaardiseerde en gevalideerde handicapscores, zoals de Expanded Disability Status Scale (EDSS) en de Timed 25-Foot Walk; en onderzoek van gezichtsvermogen en gezichtsscherpte. Het onderzoek van dr. Satyanarayan zal zowel prospectieve gegevens (gegevens gericht op het heden en de toekomst) als retrospectieve gegevens (gegevens gericht op het verleden) omvatten en zal gegevens bevatten van drie academische medische centra: het Mount Sinai Hospital, de University of Southern California en Massachusetts. Algemeen ziekenhuis. Meer over het onderzoek kunt u te weten komen via de presentatie van Dr. Satyanarayan bekijken op het 2021 Rare Neuroimmuno Disorders Symposium (RNDS).
We kijken ernaar uit om meer te leren over de impact van gezondheidsverschillen bij mensen met NMOSD uit het onderzoek van Dr. Satyanarayan, en we hebben goede hoop dat dit zal leiden tot betere zorg voor mensen in de NMOSD-gemeenschap.
SRNA James T. Lubin-beurs
Naast een deel van het hierboven beschreven onderzoek blijven we ons inzetten voor het financieren van Fellowships om klinische wetenschappers op te leiden in zeldzame neuro-immuunziekten.
In 2023, Dr. Haiwen Chen begon haar fellowship aan de Johns Hopkins University onder het mentorschap van Dr. Carlos Pardo. Dr. Chen is een kinderneuroloog en neurowetenschapper die haar medische graad behaalde aan de Universiteit van Maryland. Vervolgens voltooide ze een residentie voor kindergeneeskunde in het Johns Hopkins Hospital in Baltimore, Maryland. Ze is geïnteresseerd in het begrijpen hoe MOGAD neuronen en oligodendrocyten beïnvloedt en neurologische disfunctie veroorzaakt. Om dit te doen ontwikkelt ze een in vitro modelsysteem van neuronen en glia om te testen hoe deze worden verstoord door MOGAD auto-antilichamen en de bijbehorende ontstekingsreactie, waarbij macrofagen, T-cellen, B-cellen complementeren en microgliale activatie door cytokine-afgifte. zijn er allemaal bij betrokken.
Als we dit proces begrijpen, kunnen we beter begrijpen hoe MOGAD disfunctie van de hersenen en de wervelkolom veroorzaakt. We kunnen dan op intelligente wijze betere strategieën ontwerpen om de ziekte te behandelen. Als we bijvoorbeeld begrijpen welk deel van het immuunsysteem mogelijk overactief is bij MOGAD, kunnen we ons selectief richten op en onderdrukken van dat specifieke onderdeel van het immuunsysteem om ziekten te verzachten. Bovendien zal het team immunologische en metagenomische technologieën gebruiken om te zoeken naar gelijktijdige infecties bij patiënten met MOGAD om te onderzoeken of infecties immuunreacties kunnen veroorzaken die aanvankelijk bedoeld waren om infecties te bestrijden die vervolgens ook de lichaamseigen cellen aanvallen en auto-immuunziekten, oftewel MOGAD, veroorzaken. Ze veronderstellen dat het type trigger voor de ziekte, samen met de kenmerken van het auto-antilichaam bij individuele patiënten, zoals waar het bindt en hoe sterk het bindt, inzicht kan verschaffen in het klinische beloop van de ziekte. Ten slotte zal het team onderzoeken waarom patiënten een verschillende ernst van de ziekte, een verschillende mate van terugval en een verschillende respons op behandelingen ontwikkelen. Ze voorspellen dat deze klinische kenmerken verband kunnen houden met de mate waarin de hersenceldysfunctie door de ziekte wordt veroorzaakt en met de manier waarop de ziekte wordt veroorzaakt. Een beter begrip van hoe deze klinische verschillen ontstaan, zal ons in staat stellen patiënten beter te adviseren over de prognose en het ziekteverloop. Bovendien zouden voorspellers voor de ernst van het klinische beloop waarschijnlijk de managementkeuzes beïnvloeden in termen van hoe agressief de ziekte moet worden behandeld om de neurologische invaliditeit te minimaliseren en tegelijkertijd de mogelijke risico's van verschillende behandelingskuren in evenwicht te brengen.
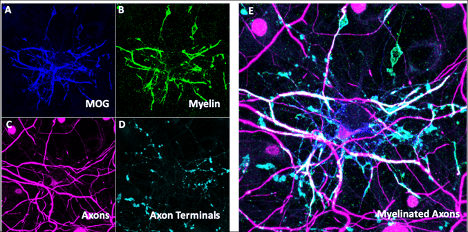
Figuurlegenda: In vitro-model van gemyeliniseerde neuronen. Immunohistochemie die de aanwezigheid aantoont van oligodendrocyten gelabeld door MOG (A) en MBP (B) en neuronen gelabeld met NF-H (C) en vGlut1 (D) met samengesteld beeld (E) dat hun overlap laat zien die gemyeliniseerde segmenten van de axonen van neuronen vertegenwoordigt.
Door SRNA geleid onderzoek
SRNA-register
Het doel van de SRNA-register dat in 2016 is gestart, is bedoeld om het onderzoek naar zeldzame neuro-immuunziekten vooruit te helpen, samen te werken met onderzoekers van over de hele wereld en deelnemers voor klinische onderzoeken te identificeren.
Sinds december 2023 hebben 711 mensen deelgenomen aan de registratie. We hebben onlangs ook een longitudinaal onderdeel aan het register toegevoegd, dat deelnemers jaarlijks moeten invullen. Dit onderdeel is belangrijk omdat de diagnose van mensen soms verandert, en we willen meten of er veranderingen zijn in iemands medicijnen en de kwaliteit van leven.
In december 2023 was bij 68% van de respondenten transversale myelitis vastgesteld, bij 10% neuromyelitis optica spectrumstoornis, bij 4% acute gedissemineerde encefalomyelitis, bij 4% acute slappe myelitis en bij 9% MOG-antilichaamziekte, en bij 4% bij een andere ziekte of ziekte. moet nog een diagnose krijgen.
Bij 35% werd de diagnose minder dan een week na het begin van de symptomen gesteld, maar bij 32% van de respondenten duurde het langer dan zes weken voordat de diagnose werd gesteld. 83% van de deelnemers kreeg behandeling na hun eerste acute aanval. Van degenen die een eerste acute behandeling kregen, kreeg echter slechts 33% van de deelnemers een tweede behandeling die anders was dan de eerste. 76% van de deelnemers kreeg revalidatietherapie.
79% van de deelnemers heeft momenteel last van zwakte of verlamming, 78% van de deelnemers heeft gevoelloosheid of verlies van gevoel, en 62% van de deelnemers heeft spasticiteit of ongecontroleerde spierspasmen. 54% ervaart nek- of rugpijn, 76% van de deelnemers ervaart neuropathische pijn en 69% van de deelnemers heeft blaas- en/of darmklachten.
Kwaliteit van leven (KvL) en voortdurend zorgbeheer bij mensen met neuromyelitis opticaspectrumstoornis (NMOSD)
Het primaire doel van deze studie is het begrijpen van de ervaringen en percepties van mensen met NMOSD of hun zorgpartners over hun kwaliteit van leven in relatie tot hun voortdurende zorgmanagement, inclusief toegang tot medische zorg, behandelingen en mogelijke barrières die zij ervaren tijdens de behandeling. hun leven in relatie tot hun stoornis.
We hebben de volgende vragen onderzocht:
- Hoe ervaren mensen met NMOSD of hun zorgpartners de kwaliteit van leven?
- Hoe ziet het voortdurende zorgtraject eruit voor mensen met NMOSD?
- Hoe kunnen we nieuwe programma’s en diensten ontwerpen die de kwaliteit van leven van mensen met NMOSD verbeteren in relatie tot doorlopende zorg?
Voor zover wij weten, zijn er geen gepubliceerde kwalitatieve onderzoeken die door patiënten gerapporteerde uitkomsten (PRO’s) gebruiken via een mensgericht ontwerpproces om de perceptie van kwaliteit van leven bij mensen met zeldzame neuro-immuunziekten in relatie tot hun voortdurende zorg te identificeren. De kernprincipes van mensgericht ontwerpen omvatten de volgende opeenvolgende stappen: empathie met alle belanghebbenden; definieer het probleem; met een open geest ideeën bedenken; prototype-oplossingen; en testen. Onze toepassing van mensgericht ontwerpen is gebaseerd op het raamwerk van Grounded Theory, waarin thema's worden geïdentificeerd tijdens een reeks interviews, praktische activiteiten (bijvoorbeeld een dagboekstudie), een ideation-sessie en een prototype-reviewsessie. Een ideatiesessie is een proces waarbij ideeën worden gegenereerd via een groepssessie die visuele activiteiten omvat met anderen met de diagnose NMOSD. Het begrijpen van de triggers en percepties van kwaliteit van leven is belangrijk voor ons werk als organisatie om zo goed mogelijk tegemoet te komen aan de behoeften van onze patiëntengemeenschap en om samen oplossingen te ontwikkelen om het lopende zorgmanagement te verbeteren.
We lieten in totaal 58 mensen de screener invullen, en 12 werden geïnterviewd door onderzoekspersoneel. Vervolgens hebben we in totaal vier ideatiesessies gehouden, drie met personen met NMOSD (n=4) en één met medische professionals die patiënten met NMOSD zien (n=11). Op basis van de discussies tijdens de ideeënsessie creëerde het onderzoeksteam een ‘patiëntenreis’. We hebben dit patiënttraject gedeeld in prototypesessies met 3 personen met NMOSD en zullen de resultaten publiceren